

電気分解はなぜ起こる?仕組みを小学生でもわかるように解説
電気分解と聞くと、なんだか実験用の道具や、むずかしい化学式を思い浮かべてしまうかもしれません。
でも安心してください。
電気分解が起こる理由は、とても順序立ったシンプルな流れで説明できます。
ここでは、 電気分解がなぜ起こるのかを、 3つの工程に分けて、ひとつずつ見ていきましょう。
|
|
|
① 電気を流すと引っぱる力が生まれる
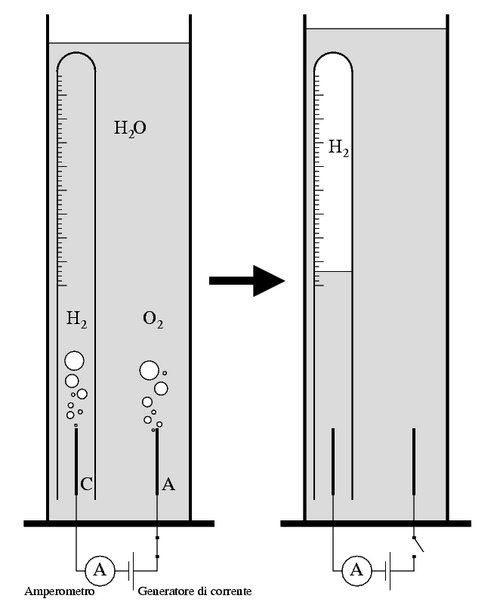
電気分解の基本メカニズムを示す模式図
外部電源で電極に電位差をかけ、溶液中のイオンを移動させる。
陰極では還元、陽極では酸化が起こり、物質が分解・生成される。
出典:『Electrolysis diagram』-Photo by Lorenzo Paulatto/Wikimedia Commons Public domain
まず最初に起こるのは、電気そのものが持っている「引っぱる力」が働き出すことです。
電気は、ただ流れるだけの存在ではありません。
物の中にある小さな粒に、しっかり影響を与えます。
![h4]()
電気の世界には、プラスとマイナスの性質があります。
この二つは、近づくと自然に引き合う関係です。
電気を流すと、プラスの力とマイナスの力がはっきりと働き始めます。
見えなくても、ちゃんと力は存在しています。
![h4]()
電気の力は、表面だけで止まりません。
水や物質の中まで届きます。
その結果、中にある小さな粒も、電気の影響を受けることになります。
![h4]()
プラスとマイナスの力がかかると、粒たちは、じっとしていられなくなります。
まだ動いてはいませんが、「動かされる準備」が整った状態。
これが、電気分解の最初のスイッチです。
② 小さな粒が左右に分かれる
次の工程では、その引っぱる力によって、粒が実際に動き始めます。
特に、水の中では、この動きが分かりやすく起こります。
![h4]()
水は、ひとつのかたまりに見えますが、中では小さな粒が集まってできています。
それぞれの粒は、プラスやマイナスの性質を持っています。
![h4]()
電気を流すと、粒たちは自分の性質に合った方向へ引かれます。
- プラスの性質をもつ粒。
- マイナスの性質をもつ粒。
それぞれが、別々の方向へ移動し始めます。
![h4]()
動いた粒は、同じ性質を持つ仲間どうしで集まります。
ばらばらだった粒が、少しずつグループを作っていく。
これが、電気によって「分けられる」動きです。
③ 集まって別の物に変わる
最後の工程では、集まった粒たちが、新しい形を作ります。
ここで、電気分解の結果がはっきり見えてきます。
![h4]()
同じ仲間どうしで集まった粒は、それぞれまとまって、形を持ち始めます。
水の場合は、
- 水素になる集まり。
- 酸素になる集まり。
が生まれます。
![h4]()
こうしてできた物は、もとの水とはまったく性質が違います。
液体だったものが、気体になる。
これが、電気分解による変化です。
![h4]()
電気は、粒を引っぱり、動かし、集める。
その結果、ひとつの物が、別の物に変わります。
電気分解とは、電気が分け役になって物を変える現象なのです。
ここまでの流れを、もう一度まとめてみましょう。
- 電気を流すと、引っぱる力が生まれる。
- 小さな粒が左右に分かれて動く。
- 集まって、別の物に変わる。
この3つの工程がつながって、電気分解は起こります。
むずかしい操作はしていません。
電気が、自分の得意な仕事を、順番にしているだけ。
そう考えると、電気分解は、とても自然でわかりやすい現象だと言えますね。
電気分解ってのはよ、「電気の力で物質を分ける仕組み」なんだぜ!水が水素と酸素に分かれるなんてまるでマジックみてぇだが、ちゃんと電気がガンガン働いてんだ、よく覚えとけよ!
|
|
|




