クーロン力と分子間力の違いは?
私たちの身の回りにある物は、ただ集まっているだけではありません。
目に見えない「力」によって、きちんと引き合い、形を保っています。
その代表が、クーロン力と分子間力。
どちらも「引き合う力」ですが、実は役割もスケールも、かなり違います。
名前が似ているせいで混同されがちですが、ここを整理すると、物質の見え方が一段クリアになります。
|
|
|
クーロン力は「電気の力」
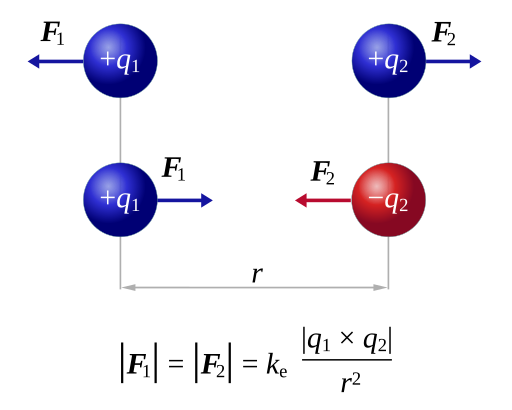
クーロン力の作用を示す図
同符号の電荷どうしが押し合い、異符号の電荷どうしが引き合う様子。空間に働く電気の力が距離や符号によって変化することを表している。
出典:Title『CoulombsLaw』-Photo by Dna-Dennis / CC BY 3.0より
クーロン力は、とてもシンプルな力です。
電気を帯びたもの同士が引き合ったり、反発したりする力。
これがクーロン力の正体です。
- プラスとマイナスは引き合う。
- 同じ符号同士は反発する。
このルール、どこかで聞いたことがありますよね。
原子の中では
- プラスの電気を持つ原子核
- マイナスの電子
が、クーロン力によって結びついています。
電子が原子核のまわりに存在できるのも、この力があるからです。
さらに、電気回路の中を電子が流れるのも、電圧という「引っ張る力」が働いているから。
つまり、電気の現象は、根っこをたどるとクーロン力に行き着きます。
まとめると── クーロン力は、電荷そのものが直接やり取りする、最も基本的な電気の力です。
原子から電気回路まで、スケールを超えて働いています。
クーロン力は電気の正体そのものなので、原子や電気現象の土台になっています!
分子間力は「分子どうしの引き合う力」
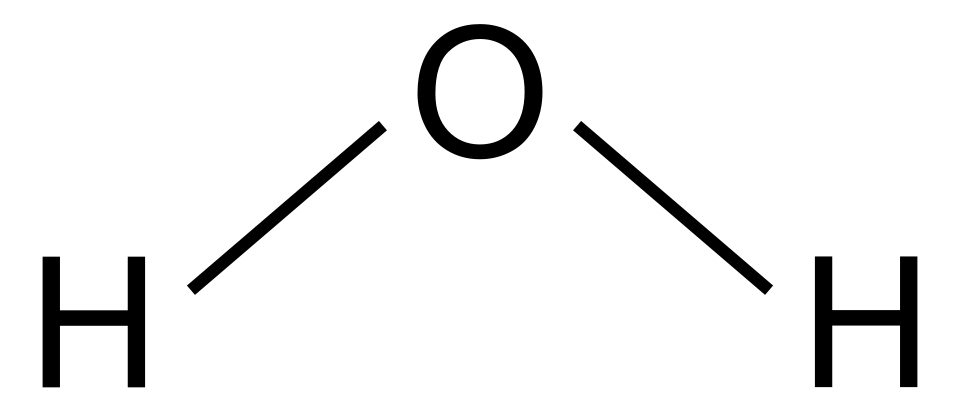
水分子(H2O)の2次元構造式
酸素原子と2つの水素原子の結合による極性をもつ構造。水は、分子同士の間に働く分子間力によって互いに引き合うことで、常温において液体の状態を保っていられる。
出典:『H2O - 2d』-Photo by Crazytonyi/Wikimedia Commons Public domain
一方で、分子間力は、もう少し控えめな力です。
その名のとおり、分子と分子のあいだで働きます。
- 水が液体でいられる理由。
- 空気中の気体が、ある程度まとまって存在できる理由。
これらを支えているのが分子間力です。
分子間力にはいくつか種類がありますが、共通しているのは、「分子の中の電気の偏り」が原因になっていること。
分子の中では、電子の分布がわずかに偏ることがあります。
その結果、分子の一部がプラス寄り、別の部分がマイナス寄りになる。
この小さな偏り同士が、引き合うことで生まれるのが分子間力です。
言い換えれば── 分子間力は、クーロン力が間接的に姿を変えて現れた力。
直接つかみ合うのではなく、そっと影響し合うイメージです。
分子間力は分子同士をゆるやかに結びつけ、物質の状態を決めています!
はたらく距離や強さがちがう
クーロン力と分子間力の最大の違いは、強さと届く距離です。
クーロン力は、とても強力。
しかも、距離が多少離れていても影響します。
原子の内部だけでなく、電線の中や空間全体で働く力です。
それに対して分子間力は、かなり近づかないと感じられません。
分子がすぐそばにあるときだけ、そっと作用する。
力の大きさも、クーロン力に比べるとずっと弱めです。
だからこそ、役割もはっきり分かれます。
- 原子や電子を支配するのがクーロン力。
- 分子の集まり方や状態を決めるのが分子間力。
──こんな具合に、担当分野が違うんですね。
端的に言えば── クーロン力は「世界の骨組み」、分子間力は「質感を決める力」。
この違いを押さえると、物質のふるまいが見えてきます。
クーロン力と分子間力は、強さと距離、そして役割がはっきり異なります!
クーロン力と分子間力は、まったく別物ではありません。
- クーロン力が、電気の基本ルール。
- 分子間力は、そのルールが分子レベルでかみ砕いて現れた姿。
つまりクーロン力と分子間力の違いは、「直接か、間接か」「強いか、控えめか」という立ち位置の違い。
そう理解すると、すっと腑に落ちます。
クーロン力と分子間力?クーロン力は“電気のガチ引力”、分子間力は“なんとな〜く引き合う磁石未満の仲良しパワー”だ!どっちも大事だけど、スケールが全然ちげぇんだよ!
|
|
|